
2023年半年报已收官,各家药企的业绩相继公开,作为经典抗肿瘤药PD-(L)1产品的业绩也陆续公布。
PD-1全称是“Programmed cell death protein1”(程序性细胞死亡蛋白1),这是表达于活化T细胞上的一个免疫检查点,肿瘤细胞表面则表达PD-1的配体PD-L1,两者结合后会抑制T细胞的活化并诱导其凋亡,使得肿瘤细胞躲开免疫系统的清除。PD-(L)1产品则可以通过激活患者自身T细胞的抗肿瘤免疫功能,发挥抗肿瘤的作用。
作为肿瘤免疫治疗的代表性产品,自2018年国内有了首个国产PD-(L)1产品后,该赛道竞争日益激烈,价格不断下降,业内人士甚至称其为“内卷之王”。根据半年报,澎湃新闻记者梳理了A股和港股10家企业的12款PD-(L)1产品销售情况,其中一半的产品未直接列出销售额,公布数据的产品中,百济神州(130.670, -1.03, -0.78%)(BGNE.NS、06160.HK、688235.SH)的PD-1产品替雷利珠单抗销售额最高,国内销售额达到18.36亿元。
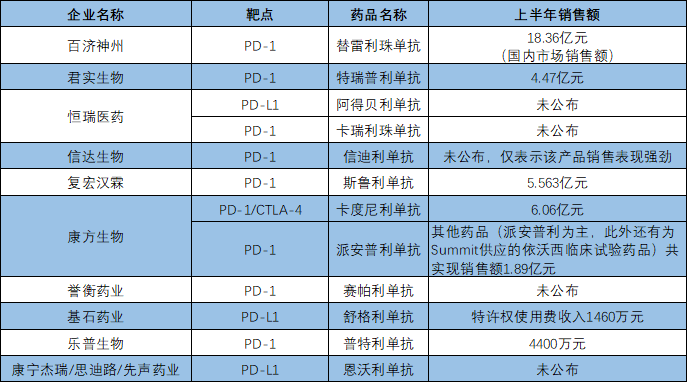 上半年PD-(L)1产品销售情况 来源:澎湃新闻记者根据半年报梳理
上半年PD-(L)1产品销售情况 来源:澎湃新闻记者根据半年报梳理
尽管竞争激烈,但从半年报来看,PD-(L)1产品依然是部分上市公司的业绩支撑,而在这类企业的布局中,不少管线仍是基于PD-(L)1产品,而PD-(L)1产品的出海之路同样被寄予厚望。
百济神州PD-1卖了18亿,多款未公布销售数据
众多PD-(L)1产品中,最先在国内获批的是君实生物(37.830, -0.26, -0.68%)(1877.HK;688180.SH)的特瑞普利单抗(商品名:拓益)。8月30日晚间,君实生物公布的2023上半年业绩显示,上半年总营收6.7亿元,其中核心产品特瑞普利单抗收入约4.47亿元,同比增长约50%。也就是说,PD-1肿瘤药一款产品贡献了上半年约66%的营收。
在PD-(L)1产品上,百济神州、恒瑞医药(41.540, 0.34, 0.83%)(600276 .SH)、信达生物(1801.HK)与君实生物共同被称为“国产PD-1四小龙”。半年报来看,恒瑞医药没有公布两款PD-(L)1产品销售情况。信达生物仅在半年报中提到,上半年产品收入24.575亿元,较去年增长20.4%,主要受益于产品组合整体销量的持续增长,包括PD-1肿瘤药信迪利单抗的强劲销售表现。不过,信达生物的合作方,即知名跨国药企礼来在二季报中提到,Tyvyt(信迪利单抗的英文商品名)上半年销售额1.646亿美元,约11.97亿元。
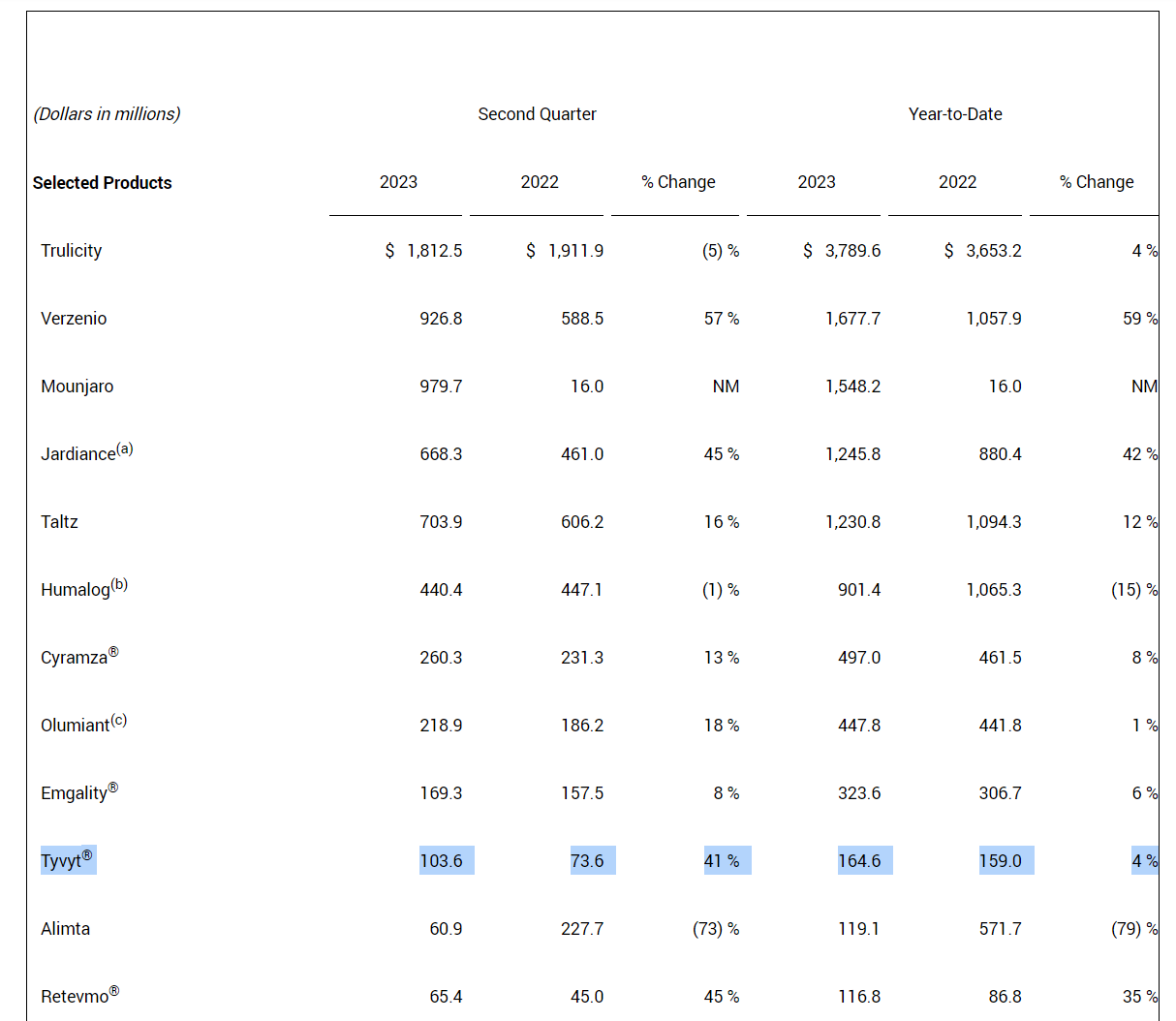 礼来二季报提到信迪利单抗的销售数据 来源:礼来二季报
礼来二季报提到信迪利单抗的销售数据 来源:礼来二季报
百济神州直接公布了替雷利珠单抗的销售额,该产品目前在中国获批,上半年国内销售额达到18.36亿元。从公开的12款产品销售数据来看,是上半年销售额之最。对于该药的增长,百济神州称,主要得益于新适应证纳入医保所带来的新增患者需求、销售团队效率的进一步提高以及药品进院数量的增加。目前,该药已在中国获批11项适应证,其中9项适应证已纳入国家医保目录。
上述“四小龙”是国内PD-(L)1产品的第一梯队,第二梯队中誉衡药业(2.170, -0.02, -0.91%)和康宁杰瑞等并未公布PD-(L)产品的销售情况,表现不一。
具体来看,康方生物(9926.HK)的PD-1/CTLA双抗肿瘤药卡度尼利单抗上半年销售额6.06亿元,其他产品销售额1.889亿元,同比下降36.4%。其他产品包括派安普利单抗注射液以及公司已与SUMMIT达成战略合作,为SUMMIT供应依沃西(AK112,PD–1/VEGF)临床试验药品。
复宏汉霖(2696.HK)的PD-1产品斯鲁利单抗被称为“H药”,上半年销售额5.563亿元。2023年3月,该产品首次实现中国境内(不包含港澳台地区)单月销售额过亿。此外,乐普生物(2157.HK)上半年PD-1产品普特利单抗销售收入为4400万元,基石药业(2616.HK)的舒格利单抗特许权使用费收入为1462万元。
有药企舍弃PD-1产品,有药企加码出海
今年6月,嘉和生物(6998.HK)在港交所公告称,旗下PD-1杰诺单抗(GB226)的新药上市申请未获批准。这是首次被拒批的国产PD-1,也被视为PD-1神药光环消失的代表性事件。除了被拒的未上市产品,还有公司放弃已上市的PD-1产品。
6月28日,誉衡药业(002437.SZ)公告称,拟将持有的参股公司广州誉衡生物科技有限公司(简称誉衡生物)42.12% 股权以2.4亿元的交易价格出售给青岛普晟普利企业管理中心(有限合伙),本次交易完成后,公司将不再持有誉衡生物股权。
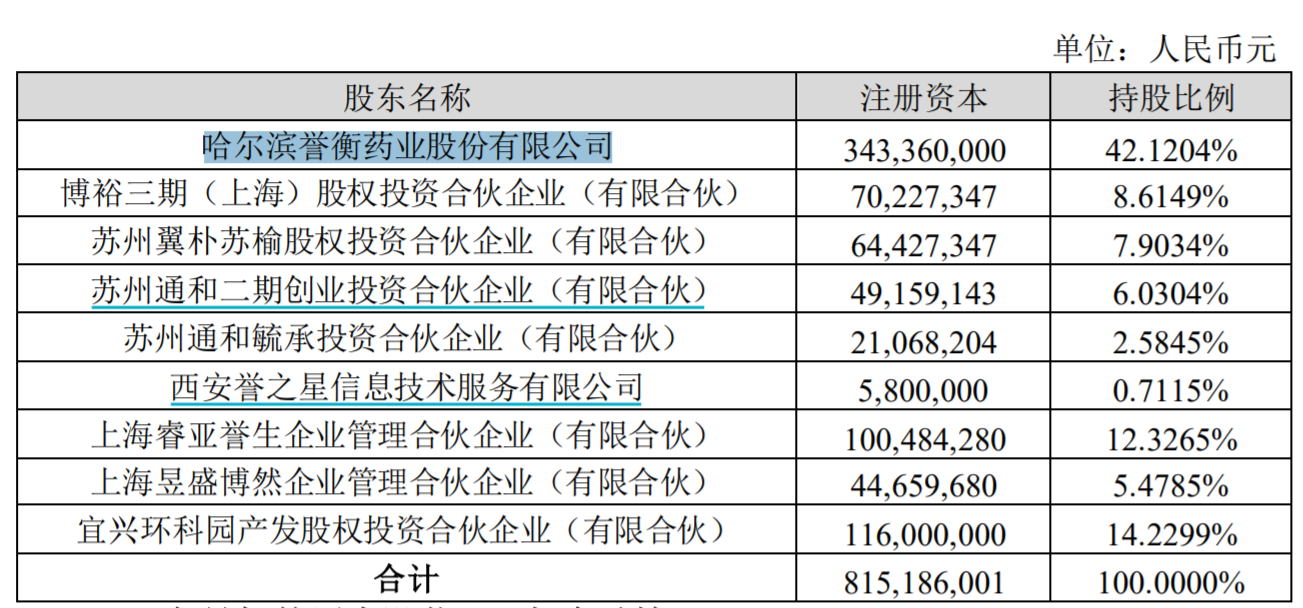 誉衡生物股权结构
誉衡生物股权结构
2016年3月,誉衡药业设立誉衡生物,将其作为未来发展生物药战略的平台载体。不到十年,为何放弃誉衡生物?誉衡药业给出的原因是鉴于誉衡生物亏损对公司业绩构成较大影响,公司结合实际情况综合评估,而“综合评估”就包括对PD-(L)1赛道的激烈竞争。
誉衡药业称,2022年底,由于誉衡生物产品销售业绩未达预期,公司对誉衡生物开发支出计提减值准备42347.79万元,影响公司净利润-17836.89万元。 2023年,国内生物药行业竞争持续加剧,国内已有多款PD-1/PD-L1相关产品获批上市,誉衡生物的赛帕利单抗注射液在市场准入、价格竞争及患者群体规模上已不具备优势;此外,誉衡生物PD-1产品宫颈癌适应证及其他产品的研发进展较为缓慢,后续发展需要更多的资金投入。
2022年报显示,截至报告期末,誉衡生物已初步完成商业化团队的组建,营销中心员工达185名。赛帕利单抗注射液已覆盖超过260家医院的患者,累计发货超过10000支。
有的PD-(L)成弃子,有的仍然在药企管线中占据着不可取代的重要。以君实生物的特瑞普利单抗为例,作为首个我国自主研发并获NMPA批准上市的PD-1产品,也是首个领衔“闯关”美国FDA的国产PD-1。在美国,特瑞普利单抗联合吉西他滨/顺铂作为晚期复发或转移性鼻咽癌患者的一线治疗,以及单药用于复发或转移性鼻咽癌含铂治疗后的二线及以上治疗的上市申请(BLA)正在接受FDA审评。
君实生物称,目前FDA已完成对生产基地的现场核查,特瑞普利单抗于美国的上市申请进展顺利。如顺利获批,君实生物北美合作伙伴Coherus将尽快在美国市场推出特瑞普利单抗。特瑞普利单抗也将成为美国首个且唯一用于鼻咽癌治疗的肿瘤免疫药物。
基石药业在半年报也提到,旗下舒格利单抗五项新药上市申请正在审评中,其中两项申请分别在英国和欧盟,适应证为一线IV期非小细胞肺癌,目前进展顺利,并已收到欧洲药品管理局发出的药物临床试验质量管理规范(GCP)检查通知;另外三项在中国大陆,适应证覆盖一线胃癌、一线食管癌、淋巴瘤。五项申请预计将在2023年下半年至2024年上半年陆续获批。
值得一提的是,各家药企在PD-1的国内商业化上也展示出不同的策略。以国家医保目录为例,恒瑞医药、百济神州等多家药企的PD-1通过谈判进入医保。也有企业选择医保外路径,如康方生物在半年报中提到,卡度尼利单抗注射液已被纳入北京、上海、杭州、成都等40多个地区惠民保目录。
在9月3日国家医保局公布的2023年医保目录调整通过形式审查药品名单中,恒瑞医药的阿得贝利单抗、乐普生物的普特利单抗、复宏汉霖的斯鲁利单抗等均不在其中,预计将不参加今年医保谈判。
- 12款国产PD-1上半年成绩单:有药企卖出18亿元,也有药企选择退出2023-09-05
- 华为Mate 60 Pro上架即售罄!多地消费者排队取机 现场激活防“黄牛”加价2023-09-04
- 政策持续出台港股内外资分歧仍明显 机构看好这几个板块2023-09-04
- 防止假冒国企央企等违法行为 企业名称登记管理新规10月施行2023-09-01
- 台风“苏拉”今日登陆,深圳等广东七市已宣布实行“五停”2023-09-01
- 央行:金融支持民企有关文件已形成初稿,持续提高民企贷款占比2023-08-31
- 最新推荐
- TOP+
- 1让员工加班,去哪儿网被罚了,网友直呼“干得漂亮!”
- 2线上禁售?下单充电盒到手电子烟,“悦刻非我优惠店”挂羊头卖狗肉,未成年购买呢?
- 3无人机拍照取证被击落!深圳高端楼盘尖岗山壹号花园遭业主集体控诉!区委书记几天前刚去视察
- 4海航集团:航空主业板块实际控制权利正式移交至辽宁方大集团
- 5邯郸建投集团涉嫌违规使用“纾困债”遭质疑:用“纾困债”收购民企债权
- 6几百元的专家号竟卖到上万?这地开展医院“号贩子”专项整治
- 73700亿"猪茅"牧原股份怎么了?董事长遭监管部门约谈 两名保代也受罚
- 8仁和药业长高、生男“神器”牵出OEM乱象 四年仅一款仿制药获批一致性评价
- 9腾讯起诉抖音侵权《王者荣耀》,获赔60万?抖音:没侵权,已上诉!
- 12款国产PD-1上半年成绩单:有药企卖出18亿元,也有药企选择退出
- 华为Mate 60 Pro上架即售罄!多地消费者排队取机 现场激活防“黄牛”加价
- 政策持续出台港股内外资分歧仍明显 机构看好这几个板块
- 防止假冒国企央企等违法行为 企业名称登记管理新规10月施行
- 台风“苏拉”今日登陆,深圳等广东七市已宣布实行“五停”
- 央行:金融支持民企有关文件已形成初稿,持续提高民企贷款占比
- 王者归来!华为上半年净利大增218%,Mate 60 Pro强势刷屏!十年研发费用逼近万亿
- 公司法修订草案三审 提升中小股东地位优化公司治理结构
- 禁令下仍有培训机构卖超额课时包 专家:预收费应全额纳入监管
- 公司法修订草案三审稿进一步落实产权平等保护要求


